
|
CARDIOMIOTOMIA Y FUNDUPLICATURA POSTERIOR PARA TRATAMIENTO DE ACALASIA Dr. Rudy López*
RESUMEN La acalasia es un trastorno motor de etiología desconocida, cuya etiopatogenia deriva de una alteración neuromuscular, caracterizada por aperistalsis del cuerpo del esófago, esfinter esofágico inferior (EEI) hipertónico, falta o relajación incompleta del EEI con la deglución y presión positiva intraesofágica debido a la retención de alimentos. Se estudiaron 32 pacientes de enero de 1991 a febrero de 1996, se les realizó cardiomiotomia transabdominal y funduplicatura posterior; 11 hombres, 21 mujeres con edad promedio de 40,30 años. En orden de frecuencia, la signosintomatología se caracterizó por disfagia, regurgitación, dolor torácico y vómitos post prandiales; 21 pacientes presentaron pérdida de peso en promedio de 10,3 kg. El esofagograma, endoscopía y manometría fueron compatibles para acalasia, la miotomía efectuada en promedio fue de 6,18 cm en esófago distal y de 1,6 cm. en el segmento gástrico. La efectividad del tratamiento fue buena en 94,8% y malos resultados en 6,2%. SUMMARY Achalasia is a motility disorder of unknown etiology and patogeny come from the neuromuscular alteration characterized by aperistalsis of the body of the esophagus, hypertonic lower esophageal sphincter, incomplete relaxation of the esophageal sphincter resulting in a intraesophagus positive pressure, because there is food retained. Thirty-two patients were studied over January 1991 to February 1996, 11 men and 21 women with a men age of 40,30 years. They had treated with transabdominal myotomy and posterior funduplicature. The sintomatology was characterized in order to frecuency by dysphagia, regurgitation, chest pain, post prandial vomit, and loss weight in 21 patients with a mean of 10,3 kg. Esophagogram, endoscopy, and manometry were adviable for achalasia. Mean of myotomy length at distal esophagus and gastric portion was 6,18 cm and 1,6 cm. respectly. The treatment was good in 94,8% and had bad results in 6,2%. * Cirujano General, Servicio de Cirugía General, Clínica Ángel Foianini À Santa Cruz ¡ Bolivia PALABRAS CLAVE: Acalasia, cardiomiotomía, funduplicatura posterior.
INTRODUCCION El término acalasia introducido por Arthur Hurst en 1915 significa literalmente "FALTA DE RELAJACION" catalogado como trastorno motor primario, conocido también como megaesófago, esofagoectasia, dilatación idiopática del esófago, discinecia del esófago, etc(1,2). Tiene una baja tasa de presentación de 0,6 a 1 por 100.000 habitantes por año en adultos(2). Más frecuente en adultos jóvenes y predominio en el sexo femenino(3). Su etiología es aún desconocida, habiéndose propuesto gran cantidad de teorías sin que alguna de ellas sea considerada como factor principal. En los pacientes afectados se encontró degeneración o ausencia de células ganglionares del plexo de Auerbach (Rake en 1926), lesiones en el núcleo dorsal del vago (Kimura 1929 y Cassella 1954), hipersensibilidad a la acetilcolina (Yngelfinger 1951)(1-3), vaciamiento gástrico rápido para líquidos y tránsito intestinal acelerado, concluyendo que existe una denervación del tubo digestivo (Eckard y col 1989)(8). Otras enfermedades pueden similar acalasia como la enfermedad de Chagas, algunos tumores malignos y colagenosis(11-14). Estudios clínicos y experimentales, han demostrado que su patogenia es de origen neuromuscular, caracterizada por aperistalsis del cuerpo del esófago, EEI hipertónico, falta o relajación incompleta del EEI con la deglución y presión positiva intra-esofágica debida a la retención del alimento y saliva(15-18). Las principales complicaciones son: a) Desnutrición b) Patología pulmonar secundaria a aspiración c) Inflamación de mucosa esofágica y d) carcicoma esofágico(19,20). Esta última es la más grave y temida, descrita inicialmente por Fagge en 1872(21), relacionado con el tiempo de evolución de la enfermedad en promedio de 17 a 40 años tiene una incidencia de presentación de 0,7 a 7,7%(19-22). La disfagia es el síntoma principal (93%), seguido de la regurgitación (75%) y dolor torácico (20-30%)(3-25). Otros síntomas menos comunes incluyen halitosis, hemorragia y pérdida de peso, significando ésta última, generalmente, una enfermedad avanzada(3-18-25). La clínica apoyada por estudios radiológicos, endoscópicos y manométricos hacen el diagnostico, siendo éste ultimo examen el que da certeza diagnostica, además ayuda a diferenciar otro tipo de patologías que cursan con trastorno de la motilidad esofágica(26, 27-29-32). El manejo esta encaminado a tratar la obstrucción del esófago distal y las alternativas en el tratamiento son: a) Farmacoterapia, b) Dilatación endoscópica, c) Miotomia quirúrgica, d) Esofagectomía. La farmacoterapia actualmente tiene malos resultados, siendo los fármacos más utilizados el dinitrato de isosorbide y nifedipina, en casos específicos(3-18-34-26-35). Las dilataciones endoscópicas esofágicas forzadas, tienen resultados muy variables en relación a su efectividad; en general se informa una efectividad de 60 a 70%(36, 37). La mejor terapéutica para estos pacientes es la miotomía quirúrgica, debiendo considerar ésta como tratamiento inicial y en estadios tempranos de la enfermedad. La cardiotomía modificada de Heller, se realiza tanto por vía torácica como abdominal, proporcionando alivio sintomático en más del 90%. La miotomía se realiza en la cara anterior del esófago y estómago con una extensión de 5 a 15 cm. de longitud en el esófago, recomendándose 5 a 6 cm. y de 10 mm, sobre segmento gástrico ya que el estómago no participa en la obstrucción. La complicación tardía más frecuente es la esofagitis por reflujo gastroesofágico, siendo difícil establecer la incidencia real, dado que depende de varios factores, como son la técnica quirúrgica, longitud de la miotomía, seguimiento y método de evaluación. La importancia de anexar un procedimiento antireflujo para reducir o prevenir la incidencia de la esofagitis por reflujo es materia de controversia(26, 40-45). La Esofagectomía esta reservada para pacientes con síntomas recurrentes, después de una miotomía quirúrgica de megaesófago severo y demostración de cáncer(28, 29). El objeto de éste trabajo es informar la experiencia obtenida con la cardiomiotomia transabdominal y funduplicatura posterior, en los últimos 5 años en el departamento de cirugía del Hospital de Especialidades Centro Médico La Raza (H.E.C.M.R.) en el tratamiento de la acalasia. MATERIAL Y METODOS Previa aceptación por el comité local de investigación del Hospital de Especialidades Centro Médico La Raza (H.E.C.M.R.) se revisaron los expedientes clínicos de 48 pacientes con diagnóstico de acalasia en el periodo comprendido, desde 1 de Enero de 1991 a 28 de Febrero de 1996, con protocolo completo preoperatorio (esofagograma, manometría, endoscopía e informe histopatológico de mucosa esofágica), de los cuales se realizó cardiomiotomía transtorácica a 9 pacientes (18,75%), transabdominal en 38 (79,2%) y a un paciente se le realizó ascenso gástrico. De los 38 pacientes con abordaje abdominal a 6 se anexó funduplicatura de Nissen y a 32 pacientes (66,7%) se anexó funduplicatura posterior, siendo estos los que constituyen la base de nuestro informe (Fig. 1). Las variables tomadas en cuenta fueron la edad, sexo, antecedentes familiares de acalasia, síntomas clínicos, tiempo de evolución, hallazgos radiológicos, endoscópicos, manométricos, tratamiento médico previo, longitud de la miotomía, complicaciones trans y postoperatorias, días de estancia hospitalaria, tiempo de seguimiento postoperatorio y eficacia del tratamiento. Todo esto se consigno en una hoja de registros (anexo). El método estadístico utilizado fue el análisis de medidas de tendencia central. Técnica Quirúrgica La técnica quirúrgica utilizada fue: 1. Incisión media supraumbilical. 2. Abordaje y disección de hiato esofágico, disección de 10 cm de esófago distal.  Figura 1 3. Miotomía en la cara anterior del esófago y estómago, la cual abarca 5 a 10 cm. sobre esófago distal y 5 a 10 mm. en el segmento gástrico. Figura 1 4. Separación del plano muscular de la mucosa, incluyendo el 50% de la circunferencia esofágica. 5. Funduplicatura posterior de 220 uniendo el fondo gástrico a los bordes de la miotomía, con puntos simples y material inabsorbible (seda 000), para mantener separado el músculo incidido y al mismo tiempo evitar reflujo gastro esofágico(48-49). RESULTADOS Se revisaron los expedientes clínicos de 32 pacientes tratados con cardiomiotomía transabdominal y funduplicatura posterior, de los cuales 11 fueron hombres (34%) y 21 mujeres (66%) (Fig. 2). La edad oscilo entre 18 a 80 años, con promedio de 42,03 años, 21 pacientes (65,6%) se encontraban entre los 30 y 60 años (Fig. 3). El tiempo transcurrido entre el inicio de los síntomas y el diagnóstico varió entre 4 meses y 15 años con promedio de 4,66 años. Las manifestaciones clínicas se presentaron con la siguiente frecuencia (Fig. 4). El rango de pérdida de peso fue de 3 a 20 kg, con una media de 10,3 kg. Los hallazgos radiológicos mostraron dilatación de grados
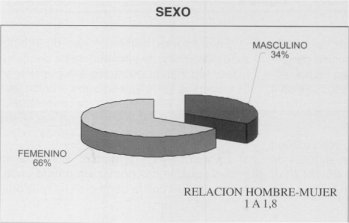 Figura 2 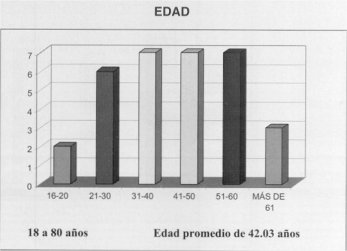 Figura 3 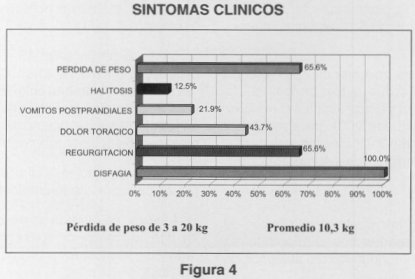 variables e imagen en punta de lápiz en la totalidad de los pacientes, retención de medio de contraste en el esófago en 26 pacientes (81,3%), terciarismo en 29 (90,6%) y en 4 pacientes (12,5%) reportaron esófago sigmoideo (Fig. 5). La endoscopía informó EEI, con facilidad para el paso del endoscopio en el 100% de los pacientes, terciarismo en 26 (81,3%), aperistaltismo en 10 (31,25%) (Fig. 6). En el informe histopatológico de la biopsia esofágica no se encontró datos de malignidad, reportando esofagitis inespecífica en 11 pacientes (34,4%), esofagitis crónica leve en 9 (28,1%), esofagitis crónica moderada en 3 (9,4%) y mucosa normal en 9 pacientes (28,1%). La manometría presentó: ausencia de ondas peristálticas primarias, falta de relajación del EEI con la deglución e hipertonia 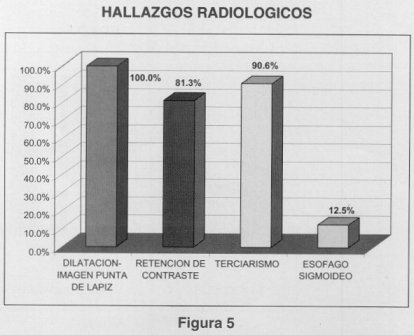 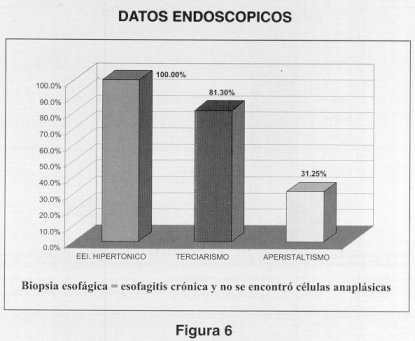 del EEI en la totalidad de los pacientes. La presión en reposo del EEI en promedio fue de 47,21 mmHg con un rango de 35 a 75 mmHg. Recibieron tratamiento médico 13 pacientes (40%), de los cuales 6 recibieron dilataciones anterógradas con sondas de Hurst, 2 recibieron calcio-antagonistas como tratamiento único y 5 pacientes recibieron ambos; los pacientes antes mencionados presentaron mejoría sintomática temporal con recurrencia rápida de los síntomas; 19 pacientes (60%) no recibieron ningún tratamiento previo. En los 32 pacientes se realizó cardiomitomía transabdominal y funduplicatura posterior como tratamiento para la acalasia. La media de la longitud de la miotomía en el segmento esofágico fue de 6,18 cm con un rango de 5 a 10 cm y en el segmento gástrico de 1,6 en promedio con rango de 1 a 2 cm. Incidentalmente se produjeron perforaciones una en el segmento esofágico y otra en el segmento gástrico en diferentes pacientes, las cuales se trataron con cierre primario con material absorvible (Vicril 000). El promedio de días de estancia hospitalaria fue de 6,15 con un rango de 4 a 10 días.
La evolución postoperatoria se controló por medio de la valoración clínica, radiológica, endoscópica y en algunos pacientes con manometría. Clínicamente se vio la desaparición de síntomas en 30 pacientes (93,7%), radiológicamente se evidenció paso libre del medio de contraste hacia el estómago en todos los pacientes y se realizó manometría en 8 pacientes, evidenciando disminución de la zona de alta presión. Se realizó seguimiento postoperatorio en promedio de 9,8 meses con un rango de 2 a 24 meses; 12 pacientes (37,5%), continúan en control. La evolución postoperatoria fue catalogada como excelente (asintomática) en 25 pacientes (78,1%), buena (disfagia ocasional) en 5 pacientes (15,7%), mala (disfagia frecuente) en 2 pacientes, los cuales requirieron dilataciones anterógradas 2 y 3 sesiones respectivamente, controlándose así, la disfagia (Fig. 7). A lo largo de ésta revisión no se evidenció mortalidad. Como resultado final, el tratamiento con miotomía transabdominal y funduplicatura posterior nos da una efectividad del 93,8% y malos resultados en 6,2%. 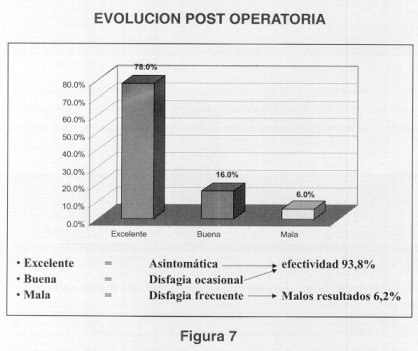 DISCUSION La etiología de la acalasia, como se describió, es desconocida aún, pero estudios clínicos y experimentales mostraron que la patogenia deriva de un trastorno neuromuscular condicionando cambios severos en el funcionamiento del esófago(30). El diagnóstico se sospecha por las manifestaciones clínicas y los hallazgos radiológicos, confirmándolo mediante la manometría. Siempre se debe realizar endoscopía con toma de biopsia de mucosa esofágica para descartar lesiones como la estenosis péptica, colagenopatías y neoplasias, además de utilizar la biopsia de mucosa con método de control para detectar carcinoma de esófago en estadio temprano, ya que se presenta en 2 a 6% de los pacientes con acalasia(21,22,23). El tratamiento de la acalasia esta encaminado solamente a aliviar la sintomatología ya que no se restablece la integridad funcional y anatómica del esófago. Con el tratamiento conservador a base de farmacoterapia y dilataciones forzadas, se encontraron resultados poco alentadores, informando una efectividad de 60 a 70% para estas últimas(26-36). El procedimiento modificado de Heller sentó las bases del tratamiento quirúrgico, el cual se puede realizar por vía torácica y/o abdominal, con miotomía de 5 a 6 cm en el esófago distal y de 5 a 10 mm en el segmento gástrico(26). En nuestra serie la miotomía practicada en el segmento esofágico fue en promedio de 6,18 cm y en el segmento gástrico fue de 1,6 cm. La necesidad de anexar un procedimiento antireflujo para disminuir o evitar la esofagitis por reflujo gastroesofágico es materia de controversia. Algunos autores como Ellis, Payne y King consideran innecesaria la funduplicatura, en forma rutinaria, ya que informan 2 a 3% de esofagitis(41,42). En contraste Belsey, Skiner, Bjurl, Jara y Nemir, informan 20 a 50% de esofagitis por reflujo si se realiza miotomía sola, concluyendo en la necesidad de anexar funduplicación(43, 44). En nuestro estudio realizamos funduplicación posterior(48), la cual además de mantener separado los bordes del músculo incidido, evita el reflujo. En los pacientes estudiados no se presentó sintomatología de reflujo gástrico, lo cual tampoco se evidencio con la serie gastro esófago duodenal postoperatoria. La efectividad de la cardiomiotomía y la funduplicatura posterior en un estudio publicado el año 1983 fue de más del 90%(49). El reflujo gastroesofágico es la complicación tardía más frecuente de la miotomía quirúrgica, siendo difícil establecer su incidencia real, debido a técnica quirúrgica, longitud de la miotomía, patologías asociadas y tipo de protocolo de seguimiento(26-40). Ellis publicó en 1993 una incidencia de esofagitis por reflujo en pacientes con miotomía transtorácica de 5% en 179 pacientes con una media de seguimiento de 9 años(51). La efectividad en nuestros pacientes fue de 93,8% con resultados pobres en 6,2%, por lo que se sugiere anexar funduplicatura a todos aquellos pacientes tratados con miotomía transabdominal. CONCLUSIONES 1. No existe evidencia clara sobre los factores etiopatogénicos y genéticos en la acalasia. 2. La edad de mayor presentación es entre los 30 y 60 años, con una edad promedio de 40,03 años y ligero predominio en el sexo femenino. 3. La evaluación diagnostica deberá incluir siempre cuadro clínico, esofagograma, endoscopía con biopsia de mucosa esofágica y manometría. 4. El tratamiento de primera intención es quirúrgico. 5. La longitud de la miotomía en promedio deberá ser de 6 a 8 cm en el esófago distal y de 5 a 10 mm en el segmento gástrico. 6. Deberá realizarse seguimiento con estudios de serie esófago gastro duodenal, tránsito esofágico con radioisótopos, pH esofágico, pH gástrico, manometría y endoscopía con tomas de biopsia de mucosa esofágica cada 2 a 3 años. 7. El tratamiento quirúrgico ofrece resultados a largo plazo, comparados con dilataciones y farmacoterapia. 8. A pesar que no encontramos neoplasias en nuestros pacientes, consideramos que todo paciente portador de acalasia, deberá tener seguimiento de por vida, ya que múltiples revisiones informan el riesgo de carcinoma de esófago. REFERENCIAS 1. Lyman A. Brewer. History of surgery of the esophagus. Am J. Surg 1989; 139:737. 2. Rickham L. Boeckman G. Achalasia in young children. Clin Pediat 1963;2:276 3. Shackerlford R. Anatomy and functional disorder of the esophagus in surgery of the alimentary trac. 3 ed, WB Saunders Co. Philadelphia 1991; vol 1:20. 4. Kaar T, Waldron R. Familiar infantile esophageal achalasia. Arch Dis Child 1991; 66: 1353. 5. Fekete G, Jacob L. Surgical treatment in 35 cases with achalasia. J. Ped Surg 1989;24:10. 6. Sonnenberg A, Massey BT,Mc Carty D, et al. Epidemiology of hospitalization for achalasia in the United States. Dig Dis Sci 1993;28:233. 7. Higgs B. Kerr F. The experimental production of the esophageal achalasia. J Thoracic Cardio surg 1965;50:16. 8. Eckard WF, Krause I, and Bolle D. Gastrointestinal transit and gastric acid secretion in patients with achalasia. Dig Dis Sci 1989;34:665. 9. Csendes A, Smok G, Braghetto I, et al. Histological studies of Auerbach┤s plexuses of the esophagus, stomach, jejenun and colon in patients with achalasia of the esophagus: Correlation with gastric acid secretion, presence of parietal cells and gastric emptying of solids. Gut 1992;33:150. 10. Mayberry J, Atkimson M. Variation in the prevalence of achalasia in Great Britain and Ireland: an epidemiological study based on hospital admission Q F Med 1987;62:67. 11. Sleissenger P, Pordtran F. Physiology and motor disorders of the esophagus in gastrointestinal disease. 4 ed. Ed. WB Saunders Co Philadelphia 1989;vol 1:541. 12. Woods C. Foutch P. Causes for secondary achalasia. Gastroenterol 1989,96:20. 13. Battle W. Rubín M. Gastro intestinal motility in amiloidosis. N. Eng Med 1979; 301: 86. 14. Arrigo R. Fritz K. Manifestaciones digestivas de la enfermedad de Chagas. Tratado de Cirugía 1 Ed. Interamericana Mexico D.F. 1989; vol 1:325. 15. Csendes A, Smok G, Braghetto I, et al. Gastroesophageal sphincter and histological changes in distal esophagus in patients with achalasia of the esophagus. Dig Dis Sci 1985;30:941. 16. Skinner B, Belsey R. Management of the esophageal motility disorders. Sauders Co 2 ed 1988:180. 17. Gaviño C, Martinez N. Acalasia del esófago. Rev Gastroenterol Mex. 1983;48(3):149. 18. Bockus H, Berck J. Achalasia of the esophagus. Gastroenterology Bockus, Sauders Co. Philp 4 ed 1985:132. 19. Schwartz-Ellis. Acalasia del esófago. Maingot Operaciones Abdominales, 8 ed. Ed. Panamericana, Buenos Aires 1989;vol 1:563. 20. Becker D, Castell D. Acute airway obstruction in achalasia, Gastroenterol 1989;97:33. 21. Hellis F, Tarshis A, Ellis FH. Carcinoma associated with achalasia. Dig Dis Sci 1984;29(11):1066. 22. Just-Viera J, Haigh C. Achalasia and carcinoma of the esophagus. Surg Gynecol obstet 1969;128:1081. 23. Goodman P, Scott L. Esophageal adenocarcinoma in patients with surgically treated achalasia. Dig Dis Sci 1990;35:1549. 24. Stretiz J, Ellis FH. Achalasia and squamus cell carcinoma of the esophagus: Anals of 241 patients. Ann Thorac Surg 1995;59(6):1604. 25. Howard P, Mather L. Five prospective study of the incidence, clinical features, and diagnosis of achalasia in Edinborg Gut 1992;33:1011. 26. Csendes A. Braguetto I, Csendes P, et al. Achalasia esophagus: Natural History and alternatives in treatment. Surgery of the esophagus, stomach and small intestine 5 ed. Ed. Litlle. Brown and co. Boston 1994:135. 27. Magover C. Altorki N. Achalasia of the esophagus. Chest Sur Clin N. Am 1994;4(4):721. 28. Millerd D, Allen M. Esophageal Resection for recurrent achalasia. Ann Thorac Surg 1995:60(4):922. 29. Peters J. Kauer W. Crookes P, et al. Esophageal resection with colon interposition for end-stage achalasia Arch Surg 1995;130:632. 30. A.S.G.E. Esophageal dilatation. Gastrointestinal Endose 1991;37(1):122. 31. Bonavina L, Nosadini A, Bardini R, et al. Primary treatment of esophageal achalasia. Arch Surg 1992;127:222. 32. Ramirez-Degollado J. Métodos de estudio del esófago. Rev. Gastroenterol Mex 1983;48(3):103. 33. Ott D, Richter J. Esophageal radiography and manometric: Correlation in 172 patients with disphagia. AJG 1987;149:307. 34. Traube M, Dubouik S. The role of Nifedipine therapy in achalasia: Results of a randomized, double.-blind, placebo-controlled study. Ann J. Gastroenterol 1989;24:1259. 35. Bartalloti M, Lbao G, Clinical and manometry effects of Nifedipine on patients with achalasia. Gastroenteology 1982:83:963. 36. Csendes A, Braghetto I, Enriquez A, Cortez C. Late result of a prospective randomized study comparing forceful dilatation and esophagumyotomy in patients with achalasia. Gut 1989;30:299. 37. Richter FE Surgery or Pneumatic dilatation for achalasia a head to head comparison. Now all the questions answered?. Gastroenterology 1989; 30: 1340. 38. Sanderson D, Ellis FH. Olsen A. Achalasia of the esophagus. Results of therapy by dilatation. Chest 1970;58:116. 39. Vantrapen G, Hellemans J, Dellof W, et al. Treatmen of achalasia with dilatation. Gut 1971;12:268. 40. Andreollo N, Earlam R. Heller┤s myotomy for achalasia: Is an added antireflux procedure necessary ?. Br J Surg 1987:74(9):765. 41. Ellis FH Crozier R. And gibb S. Re-operative achalasia surgery. J. Thorac Surg 1986;92:859. 42. Payne W. And King R. Tratment of achalasia of the esophagus. Surg Clin North Am 1983;63:963. 43. Skinner DB. Myotomy and achalasia. Ann Thorac Surg 1984;37:183. 44. Bjork S. Dervenk L, Gatzinsky P, et al. Esophagucardiomyotomy and antirrefluz procedures. Acta Chir Scand 1982;184:525. 45. Torres A, Suarez A, Fernández F, et al. Importance of an antirreflux mechanism in the surgery of the typical achalasia of the cardia. Disease of the Esophagus. Ed. AJ Siewert, AH Holscher. Berling: Springer Verlang 1988:936. 46. Mucio M, Zamora A. Acalasia tratamiento laparoscópico. Cirujano General 1993;15(4s):25. 47. Ancona E. Anselmino M. Saninotto G, et al. Esophageal achalasia Laparoscopic versus conventional open Heller-door operation. Am J Surg 1995;170(3):365. 48. Posterior U, Ramirez D, Ize L. Carrasco A. Fundamentos fisiopatológicos en el tratamiento de la acalasia del esófago. Gac Med Mex. 1973;106:399. 49. Gutiérrez C, Cervantes C, Ayala E, et al. Acalasia del esófago: Cardiomiotomia y funduplastía tratamiento quirúrgico de elección. Rev Gastroent Mex 1983;48(2):65. 50. Rosato E, Acker M. Transabdominal esophagomyotomy and partial funduplication for treatment of achalasia. Surg Gynecol Obstet 1991:173(2):137. 51. Ellis FH. Esophagomyotomy for achalasia: a 22 years experience. Br. J. Surg 1993;80:882.
|